Ácido xasmónico
| Ácido xasmónico | |
|---|---|
 | |
 | |
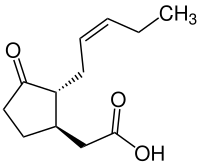
Ácido (1R,2R)-3-oxo-2-(2Z)-2-pentenil-ciclopentanoacético | |
Outros nomes (−)-Ácido xasmónico | |
| Identificadores | |
| Número CAS | 6894-38-8 |
| PubChem | 5281166 |
| ChemSpider | 4444606 |
| ChEBI | CHEBI:18292 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C12H18O3 |
| Masa molecular | 210,27 g/mol |
| Punto de ebulición | 160 °C; 320 °F; 433 K (a 0,7 mmHg) |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
O ácido xasmónico[1][2] é un derivado do ácido graxo ácido α-linolénico, que pertence á clase de hormonas de plantas chamadas xasmonatos. Biosintetízase a partir do ácido linolénico pola vía octadecanoide. O seu nome deriva da planta da especie Jasminum grandiflorum (un xasmín) da cal se illaron os xasmonatos.[3]
A principal función do ácido xasmónico e os seus varios metabolitos é regular as respostas da planta aos estreses bióticos e abióticos e o crecemento e desenvolvemento da planta.[4] Os procesos de crecemento e desenvolvemento da planta regulados inclúen a inhibición do crecemento, senescencia, enroscamento dos gabiáns[5], desenvolvemento das flores e abscisión (caída) das follas. O ácido xasmónico é tamén responsable da formación de tubérculos e bulbos na planta da pataca, iñame e cebolas. Ten un importante papel na resposta ás feridas das plantas e na resistencia adquirida sistémica. Cando as plantas son atacadas por insectos, responden liberando ácido xasmónico, que activa a expresión de inhibidores da protease, entre outros moitos compostos defensivos antiherbívoros. Estes inhibidores de proteases impiden a actividade proteolítica das proteases dixestivas dos insectos ou as súas "proteínas salivares".[6][7]
O ácido xasmónico tamén se converte nunha variedade de derivados incluíndo ésteres como o metilxasmonato, e pode tamén conxugarse con aminoácidos.
Este composto pode ter un papel no control de pragas,[8] e empezou a utilizarse en forma de spray para aplicalo ás sementes antes da súa plantación, xa que isto estimula as defensas naturais contra as pragas.
Notas
[editar | editar a fonte]- ↑ PubChem compound jasmonic acid
- ↑ ChemSpider jasmonic acid
- ↑ Demole E; Lederer, E.; Mercier, D. (1962). "Isolement et détermination de la structure du jasmonate de méthyle, constituant odorant caractéristique de l'essence de jasmin". Helv Chim Acta 45: 675–85. doi:10.1002/hlca.19620450233.
- ↑ Delker, C.; Stenzel, I.; Hause, B.; Miersch, O.; Feussner, I.; Wasternack, C. (2006). "Jasmonate Biosynthesis in Arabidopsis thaliana - Enzymes, Products, Regulation". Plant Biology 8 (3): 297–306. doi:10.1055/s-2006-923935. PMID 16807821.
- ↑ Dicionario da Real Academia Galega gabián (2ª acepción). Arquivado 22 de xullo de 2013 en Wayback Machine.
- ↑ Zavala, J. A.; Patankar, A. G.; Gase, K.; Hui, D.; Baldwin, I. T. (2004). "Manipulation of Endogenous Trypsin Proteinase Inhibitor Production in Nicotiana attenuata Demonstrates Their Function as Antiherbivore Defenses". Plant Physiology 134 (3): 1181–1190. doi:10.1104/pp.103.035634. PMC 389942. PMID 14976235.
- ↑ Lutz, Diana (2012). Key part of plants' rapid response system revealed. Washington University in St. Louis. http://news.wustl.edu/news/Pages/23979.aspx Arquivado 09 de xaneiro de 2016 en Wayback Machine.
- ↑ "Success for plants' pest control". BBC News. 2008-10-07. Consultado o 2013-04-12.
Véxase tamén
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Sankawa, Ushio; Barton, Derek H. R.; Nakanishi, Koji; Meth-Cohn, Otto, eds. (1999). Comprehensive Natural Products Chemistry : Polyketides and Other Secondary Metabolites Including Fatty Acids and Their Derivatives. Pergamon Press. ISBN 0-08-043153-4.
