Ciclooxixenase
| Prostaglandina-endoperóxido sintase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Número EC | 1.14.99.1 | ||||||||
| Número CAS | 9055-65-6 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| Gene Ontology | AmiGO / EGO | ||||||||
| |||||||||
Ciclooxixenase
| |
| Identificadores | |
| Símbolo | PTGS1 |
| Símbolos alt. | COX-1 |
| Entrez | 5742 |
| HUGO | 9604 |
| OMIM | |
| PDB | 1CQE |
| RefSeq | NM_080591 |
| UniProt | P23219 |
| Outros datos | |
| Número EC | 1.14.99.1 |
| Locus | Cr. 9 q32-q33.3 |
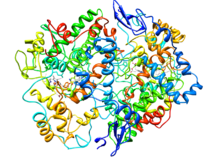
| |
Ciclooxixenase
| |
| Identificadores | |
| Símbolo | PTGS2 |
| Símbolos alt. | COX-2 |
| Entrez | 5743 |
| HUGO | 9605 |
| OMIM | |
| PDB | 6COX |
| RefSeq | NM_000963 |
| UniProt | P35354 |
| Outros datos | |
| Número EC | 1.14.99.1 |
| Locus | Cr. 1 q25.2-25.3 |
A ciclooxixenase ou cicloosixenase (COX), coñecida oficialmente como prostaglandina-endoperóxido sintase (PTGS), é un encima (EC 1.14.99.1) que é responsable da formación de prostanoides, incluíndo as prostaglandinas, as prostaciclinas e os tromboxanos.
A abreviatura "COX" para este encima atópase sobre todo na literatura médica. En xenética, o símbolo oficial é "PTGS" para a familia de xenes e proteínas da prostaglandina-endoperóxido sintase (ciclooxixenase), porque a abreviatura "COX" xa se estaba usando para a familia de xenes e proteínas da citocromo c oxidase. Os nomes "prostaglandina sintase (PHS)" e "prostaglandina endoperóxido sintetase (PES)" tamén se usan para referirse á COX.
Nos humanos existen dúas ciclooxixenases, chamadas COX-1 (ou PTGS1) e COX-2 (ou PTGS2). Existe ademais unha isoforma da COX-1, chamada COX-3 e outras dúas pequenas proteínas derivadas de COX-1 chamadas PCOX-1A e PCOX-1B.
A inhibición farmacolóxica de COX pode aliviar os síntomas da inflamación e a dor. Os fármacos antiinflamatorios non esteroides (AINEs), como a aspirina e o ibuprofeno, exercen os seus efectos por medio da inhibición das COX.
Farmacoloxía
[editar | editar a fonte]A COX-1 e a COX-2 teñen un peso molecular similar, aproximadamente de 70 e 72 kDa, respectivamente, e cun 65% de homoloxía de secuencias de aminoácidos e uns sitios catalíticos case idénticos. A diferenza máis significativa entre estes isoencimas, que permite unha inhibición selectiva de cada unha delas, é a substitución da isoleucina en posición 523 da COX-1 por unha valina na COX-2. O residuo menor Val523 de COX-2 permite o acceso a un peto lateral hidrofóbico (que a Ile523 agocha estericamente). Fármacos, como o DuP-697 e o coxibs derivados del, únense a un sitio alternativo e son considerados inhibidores selectivos de COX-2.
AINEs clásicos
[editar | editar a fonte]Os inhibidores principais de COX son os antiinflamatorios non esteroideos (AINEs).
Os inhibidores clásicos de COX non son selectivos e inhiben todos os tipos de COX. A inhibición resultante da síntese de prostaglandinas e tromboxanos ten o efecto de reducir a inflamación, e efectos antipiréticos, antitrombóticos e analxésicos. O efecto adverso máis frecuentes dos AINEs é a irritación da mucosa gástrica, xa que as prostaglandinas normalmente teñen un papel protector no tracto gastrointestinal. Algúns AINEs son tamén ácidos, o cal pode causar danos adicionais ao tracto gastrointestinal.
AINEs novos
[editar | editar a fonte]A selectividade pola COX-2 é a principal característica dos fármacos celecoxib, etoricoxib, e doutros fármacos deste tipo. Como o COX-2 é usualmente específica dos tecidos inflamados, hai moita menos irritación gástrica asociada con inhibidores de COX-2, cunha diminución do risco de úlcera péptica. A selectividade da COX-2 non parece negar outros efectos laterais dos AINEs, moi notablemente un incremento do risco de insuficiencia renal, e hai evidencias que indican un incremento do risco de ataque ao corazón, trombose, e accidente cerebrovascular por medio dun incremento do tromboxano non equilibrado pola prostaciclina (que é reducida pola inhibición da COX-2). O fármaco Rofecoxib foi retirado en 2004 debido a preocupacións sobre os seus efectos. Algúns outros AINEs selectivos da COX-2, como o celecoxib, e etoricoxib, están aínda no mercado.
Inhibición das COX natural
[editar | editar a fonte]Algúns fungos culinarios como o maitake, poden inhibir parcialmente a COX-1 e a COX-2.[1][2]
Unha variedade de flavonoides inhiben tamén a COX-2.[3]
Os aceites de peixes proporcionan ácidos graxos alternativos ao ácido araquidónico. Estes ácidos poden ser convertidos nalgunhas prostaciclinas antiinflamatorias pola COX en vez de en prostaciclinas proinflamatorias.[4]
A hiperforina inhibe a COX-1 de 3 a 18 veces máis que a aspirina.[5]
O calcitriol (vitamina D) inhibe significativamente a expresión do xene COX-2.[6]
Debe terse precaución ao combinar doses baixas de aspirina con inhibidores da COX-2 debido ao potencial incremento de danos á mucosa gástrica. A COX-2 é regulada á alza cando a COX-1 é suprimida pola aspirina, o que se cre é importante en mecanismos de potenciación da defensa das mucosas e diminúe as erosións causadas pola aspirina.[7]
Efectos laterais cardiovasculares dos inhibidores da COX
[editar | editar a fonte]Os inhibidores da COX-2 incrementan o risco de aterotrombose mesmo se se usan durante un tempo breve. Unha análise feita en 2006 de 138 ensaios aleatorizados e case 150.000 participantes[8] sacou a conclusión de que os inhibidores selectivos da COX-2 están asociados cun risco moderadamente incrementado de episodios vasculares, principalmente debido a que se duplica o risco de infarto de miocardio, e tamén a que os réximes de tratamento de altas doses dalgúns AINEs tradicionais como o diclofenac e o ibuprofeno están asociados cun incremento similar do risco de episodios vasculares.
Os aceites de peixe (por exemplo o aceite de fígado de bacallau) propuxéronse como alternativa razoable para o tratamento da artrite reumatoide e outras condicións como consecuencia do feito de que supoñen un menor risco cardiovascular que outros tratamentos incluíndo os AINESs.[4]
Notas
[editar | editar a fonte]- ↑ Zhang Y, Mills GL, Nair MG (Dec 2002). "Cyclooxygenase inhibitory and antioxidant compounds from the mycelia of the edible mushroom Grifola frondosa". Journal of Agricultural and Food Chemistry 50 (26): 7581–5. PMID 12475274. doi:10.1021/jf0257648.
- ↑ Zhang Y, Mills GL, Nair MG (2003). "Cyclooxygenase inhibitory and antioxidant compounds from the fruiting body of an edible mushroom, Agrocybe aegerita". Phytomedicine 10 (5): 386–90. PMID 12834003. doi:10.1078/0944-7113-00272.
- ↑ O'Leary KA, de Pascual-Teresa S, de Pascual-Tereasa S, Needs PW, Bao YP, O'Brien NM, Williamson G (Jul 2004). "Effect of flavonoids and vitamin E on cyclooxygenase-2 (COX-2) transcription". Mutation Research 551 (1-2): 245–54. PMID 15225597. doi:10.1016/j.mrfmmm.2004.01.015.
- ↑ 4,0 4,1 Cleland LG, James MJ, Proudman SM (2006). "Fish oil: what the prescriber needs to know". Arthritis Research & Therapy 8 (1): 202. PMC 1526555. PMID 16542466. doi:10.1186/ar1876.
- ↑ Albert D, Zündorf I, Dingermann T, Müller WE, Steinhilber D, Werz O (Dec 2002). "Hyperforin is a dual inhibitor of cyclooxygenase-1 and 5-lipoxygenase". Biochemical Pharmacology 64 (12): 1767−75. PMID 12445866.
- ↑ Moreno J, Krishnan AV, Peehl DM, Feldman D (July–August 2006). "Mechanisms of vitamin D-mediated growth inhibition in prostate cancer cells: inhibition of the prostaglandin pathway". Anticancer Research 26 (4A): 2525–30. PMID 16886660.
- ↑ Wallace JL (Oct 2008). "Prostaglandins, NSAIDs, and gastric mucosal protection: why doesn't the stomach digest itself?". Physiological Reviews 88 (4): 1547–65. PMID 18923189. doi:10.1152/physrev.00004.2008.[Ligazón morta]
- ↑ Kearney PM, Baigent C, Godwin J, Halls H, Emberson JR, Patrono C (Jun 2006). "Do selective cyclo-oxygenase-2 inhibitors and traditional non-steroidal anti-inflammatory drugs increase the risk of atherothrombosis? Meta-analysis of randomised trials". Bmj 332 (7553): 1302–8. PMC 1473048. PMID 16740558. doi:10.1136/bmj.332.7553.1302.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- A proteína cilooxixenase
- Cyclooxygenase Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- GONUTS Page: Cyclooxygenase
- Cyclooxygenase: Proteopedia, life in 3D
- Discusión domecanismo encimático con modelos interactivos 3D
