Alfa-queratina
A alfa-queratina (α-queratina), é un tipo de proteína queratina que se encontra nos mamíferos. Esta proteína é o principal compoñente do pelo, cornos, uñas e a capa epidérmica da pel. A α-queratina é unha proteína estrutural fibrosa, xa que os seus aminoácidos forman unha estrutura secundaria repetida. A estrutura secundaria da α-queratina é moi similar á das proteínas típicas en hélice α e forma unha hélice superenrolada.[1] Debido á súa estrutura apertadamente enrolada, pode funcionar como un dos materiais biolóxicos máis fortes e ten varios usos nos mamíferos, desde a de formar gadoupas predadoras a pelos para abrigarse. A α-queratina sintetízase polos procedementos normais, pero cando a célula madura está chea de α-queratina, e morre, creando unha forte unidade non vascularizada de tecido queratinizado.[2]
Estrutura
[editar | editar a fonte]
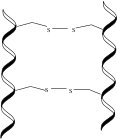
A α-queratina é unha cadea polipeptídica, rica en alanina, leucina, arxinina e cisteína, que forma unha hélice α dextroxira.[3][4] Dúas destas cadeas polipeptídicas enrólanse entre si formando unha estrutura helicoidal levoxira chamada hélice suerenrolada. As cadeas do dímero, de aproximadamente 45 nm de longo, están unidas por medio de pontes disulfuro entre as moitas cisteínas que se encontran na proteína.[2] Os dímeros despois alíñanse, e os seus extremos C-terminal enlázanse cos extremos N-terminal doutros dímeros, e dúas destas novas cadeas únense en sentido lonxitudinal, sempre por medio de pontes disulfuro, para formar un protofilamento.[5] Dous protofilamentos agréganse para formar unha protofibrila, e catro protofibrilas polimerízanse para formar os filamentos intermedios, que son a subunidde básica das α-queratinas. Estes filamentos intermedios poden condensar nunha formación en hélice superenrolada duns 7 nm de diámetro, e pode ser de tipo I, ácida, ou de tipo II, básica. Os filamentos intermedios están finalmente incrustados nunha matriz de queratina que ou ben ten un alto contido de residuos de cisteína ou ben de glicina, tirosina e fenilalanina. Os diferentes tipos, aliñamentos e matrices destes filamentos intermedios explican a gran variedade de estruturas de α-queratina, con distintas propiedades, que se encontra en mamíferos.[6]
Bioquímica
[editar | editar a fonte]Síntese
[editar | editar a fonte]A síntese de α-queratina empeza preto dos puntos de adhesións focais na membrana da célula. Alí, os precursores dos filamentos de queratina pasan por un proceso coñecido como nucleación, no que os precursores dos dímeros e filamentos se alongan, fusionan e agrupan.[2] A medida que ocorre esta síntese, os precursores dos filamentos de queratina son transportados polas fibras de actina da célula cara ao núcleo celular. Alí, os filamentos intermedios de alfa-queratina xúntanse e forman redes de estrutura diferentes segundo o uso que van ter as células queratina a medida que simultameamente se degrada o seu núcleo.[7] Porén, se é preciso, en vez de continuaren crecendo, os complexos de queratina desensámblanse orixinando precursores de queratina non filamentosos que poden difundir polo citoplasma da célula. Estes filamentos de queratina poderán usarse na futura síntese de queratina, ou reorganizar a estrutura final ou crear un complexo de queratina diferente. Cando a célula se encheu coa queratina correcta e estruturada debidamente, experimenta unha estabiliación da queratina e a célula morre, o que é unha forma de morte celular programada. Isto ten como resltado unha célula queratiniada non vascular completamente madura.[8] Estas células con alfa-queratina completamente maduras ou células cornificadas son os principais compoñentes do pelo, a capa externa das uñas e cornos e a capa epidérmica da pel.[9]
Propiedades
[editar | editar a fonte]A propiedade de maior importancia biolóxica da alfa-queratina é a súa estabilidade estrutural. Cando están sometidas a un estrés mecánico, as estruturas da α-queratina poden reter a súa forma e así poden protexer o que as rodea.[10] Baixo unha tensión alta, a alfa-queratina pode incluso cambiar a beta-queratina, unha formación de queratina aínda máis forte que ten unha estrutra secundaria de folla beta.[11] Os tecidos de alfa-queratina tamén mostran signos de viscoelasticidade, permitíndolles estirarse e absorber impactos ata un certo grao, pero poden tamén acabar fracturándose. A forza da alfa-queratina tamén se ve afectada polo contido de auga na matriz dos filamentos intermedios; un maior contido de auga diminúe a forza e a rixidez das células queratinizadas debido aos seus efectos sobre as pontes de hidróxeno na rede da proteína.[2]
Tipos
[editar | editar a fonte]Tipo I e tipo II
[editar | editar a fonte]As proteínas alfa-queratinas poden ser de dous tipos: tipo I ou tipo II. Hai 54 xenes de queratina nos humanos, 28 dos cales codifican o tipo I, e 26 o tipo II.[12] As proteínas de tipo I son ácidas, o que significa que conteñen máis aminoácidos ácidos, como o ácido aspártico, mentres que as do tipo II son básicas, o que significa que conteñen máis aminoácios básicos, como a lisina.[13] Esta diferenciación é especialmente importante nas alfa-queratinas porque na síntese do seu dímero subunidade, a hélice superenrolada, unha das proteínas enroladas que o forman debe ser de tipo I, mentres que a outra debe ser de tipo II.[2] Incluso dentro dos tipos I e II, hai queratinas ácidas e básicas que son especialmente complementarias entre si en cada organismo. Por exemplo, na pel humana, a K5, é un tipo de alfa-queratina de tipo II, que se emparella principalmente coa K14, que é de tipo I, para formar o complexo de alfa-queratina das células da epiderme da pel.[14]
Dura e branda
[editar | editar a fonte]As alfa-queratinas duras, como as que forman as uñas, teñen un maior contido en cisteína na súa estrutura primaria. Isto causa un incrementeo de pontes disulfuro que poden estabilizar a estrutura da queratina, permitíndollo resistir unha forza elevada antes de fracturarse. Por outra parte, as alfa-queratinas brandas, como as que se encontran na pel, conteñen unha cantidade comparativaemtne pequena de pontes disulfuro, o que fai a súa estrutura máis flexible.[1]
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 G.,, Voet, Judith; W.,, Pratt, Charlotte. Fundamentals of biochemistry : life at the molecular level. ISBN 9781118918401. OCLC 910538334.
- ↑ 2,0 2,1 2,2 2,3 2,4 Wang, Bin; Yang, Wen; McKittrick, Joanna; Meyers, Marc André (2016-03-01). "Keratin: Structure, mechanical properties, occurrence in biological organisms, and efforts at bioinspiration". Progress in Materials Science 76: 229–318. doi:10.1016/j.pmatsci.2015.06.001.
- ↑ Burkhard, Peter; Stetefeld, Jörg; Strelkov, Sergei V. "Coiled coils: a highly versatile protein folding motif". Trends in Cell Biology 11 (2): 82–88. doi:10.1016/s0962-8924(00)01898-5.
- ↑ Pace, C N; Scholtz, J M (1998-07-01). "A helix propensity scale based on experimental studies of peptides and proteins.". Biophysical Journal 75 (1): 422–427. ISSN 0006-3495. PMC 1299714. PMID 9649402.
- ↑ Steinert, Peter M.; Steven, Alasdair C.; Roop, Dennis R. "The molecular biology of intermediate filaments". Cell 42 (2): 411–419. doi:10.1016/0092-8674(85)90098-4.
- ↑ McKittrick, J.; Chen, P.-Y.; Bodde, S. G.; Yang, W.; Novitskaya, E. E.; Meyers, M. A. (2012-04-03). "The Structure, Functions, and Mechanical Properties of Keratin". JOM (en inglés) 64 (4): 449–468. ISSN 1047-4838. doi:10.1007/s11837-012-0302-8.
- ↑ Windoffer, Reinhard; Beil, Michael; Magin, Thomas M.; Leube, Rudolf E. (2011-09-05). "Cytoskeleton in motion: the dynamics of keratin intermediate filaments in epithelia". The Journal of Cell Biology (en inglés) 194 (5): 669–678. ISSN 0021-9525. PMID 21893596. doi:10.1083/jcb.201008095.
- ↑ Kölsch, Anne; Windoffer, Reinhard; Würflinger, Thomas; Aach, Til; Leube, Rudolf E. (2010-07-01). "The keratin-filament cycle of assembly and disassembly". J Cell Sci (en inglés) 123 (13): 2266–2272. ISSN 0021-9533. PMID 20554896. doi:10.1242/jcs.068080.
- ↑ Eckhart, Leopold; Lippens, Saskia; Tschachler, Erwin; Declercq, Wim (2013-12-01). "Cell death by cornification". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research 1833 (12): 3471–3480. doi:10.1016/j.bbamcr.2013.06.010.
- ↑ Pan, Xiaoou; Hobbs, Ryan P; Coulombe, Pierre A. "The expanding significance of keratin intermediate filaments in normal and diseased epithelia". Current Opinion in Cell Biology 25 (1): 47–56. PMID 23270662. doi:10.1016/j.ceb.2012.10.018.
- ↑ Kreplak, L.; Doucet, J.; Dumas, P.; Briki, F. (2004-07-01). "New Aspects of the α-Helix to β-Sheet Transition in Stretched Hard α-Keratin Fibers". Biophysical Journal (en inglés) 87 (1): 640–647. PMC 1304386. PMID 15240497. doi:10.1529/biophysj.103.036749.
- ↑ Moll, Roland; Divo, Markus; Langbein, Lutz (2017-03-07). "The human keratins: biology and pathology". Histochemistry and Cell Biology 129 (6): 705–733. ISSN 0948-6143. PMC 2386534. PMID 18461349. doi:10.1007/s00418-008-0435-6.
- ↑ Strnad, Pavel; Usachov, Valentyn; Debes, Cedric; Gräter, Frauke; Parry, David A. D.; Omary, M. Bishr (2011-12-15). "Unique amino acid signatures that are evolutionarily conserved distinguish simple-type, epidermal and hair keratins". Journal of Cell Science 124 (24): 4221–4232. ISSN 0021-9533. PMC 3258107. PMID 22215855. doi:10.1242/jcs.089516.
- ↑ Lee, Chang-Hun; Coulombe, Pierre A. (2009-08-10). "Self-organization of keratin intermediate filaments into cross-linked networks". The Journal of Cell Biology (en inglés) 186 (3): 409–421. ISSN 0021-9525. PMC 2728393. PMID 19651890. doi:10.1083/jcb.200810196.
