Colestano
| Colestano | |
|---|---|
 | |
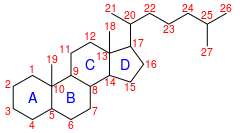 | |
Colestano | |
(1R,3aS,3bR,9aS,9bS,11aR)-9a,11a-Dimetil-1-[(2R)-6-metilheptan-2-il]hexadecahidro-1H-ciclopenta[a]fenantreno | |
| Identificadores | |
| Número CAS | 14982-53-7 5α/β, 481-21-0 5α, 481-20-9 5β |
| PubChem | 6857534 |
| ChemSpider | 5256870 |
| ChEBI | CHEBI:35516 |
| Ligando IUPHAR | 2802 |
| Imaxes 3D Jmol | Image 1 Image 2 |
| |
| |
| Propiedades | |
| Fórmula molecular | C27H48 |
| Masa molar | 372,67 g mol−1 |
| Densidade | 0,911 g/ml |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
O colestano é un triterpeno tetracíclico saturado. Este biomarcador de 27 carbonos prodúcese por diaxénese do colesterol e é un dos biomarcadores máis abundantes no rexistro xeolóxico.[2] A presenza de colestano, os seus derivados e compostos químicos relacionados en mostras ambientais é interpretado comunmente como un indicador de vida animal ou de trazas de O2, xa que os animais son os que case exclusivamente producen colesterol, e por iso foi usado para establecer as relacións evolutivas entre organismos antigos de orixe filoxenética descoñecida e os taxons modernos de metazoos.[3] O colesterol é producido con menor abundancia por outros organismos (por exemplo, rodófitas, plantas terrestres), pero como estes outros organismos producen diversos esterois non pode usarse como un indicador concluínte de ningún deses taxons.[4][5] Atópase a miúdo en análises de compostos orgánicos no petróleo.
Introdución
[editar | editar a fonte]O colestano é un biomarcador animal de 27 carbonos saturado que se atopa con frecuencia nos depósitos de petróleo. É un produto diaxenético do colesterol, que é unha molécula orgánica feita principalmente polos animais e constitúe ~30 % en peso da membrana plasmática da célula animal (nas membranas subcelulares é moi escaso). O colesterol é responsable do grao de rixidez ou fluidez da membrana, así como do transporte intracelular, sinalización celular e condución nerviosa.[6] En humanos é tamén o precursor de hormonas (como estróxenos ou testosterona). É sintetizado por medio do escualeno e adopta de forma natural unha orientación estereoquímica específica (3β-ol, 5α (H), 14α (H), 17α (H), 20R). Esta orientación estereoqímica mantense normalmente despois dos procesos diaxenéticos, pero o colestano pode encontrarse no rexistro fósil con moitas configuracións estereoquímicas.
Biomarcador
[editar | editar a fonte]O colestano no rexistro fósil adoita interpretarse como un biomarcador indicador de antiga vida animal e a miúdo utilízano os xeoquímicos para reconstruír a evolución animal (especialmente no Precámbrico; por exemplo, no Ediacárico,[3] Crioxénico e Proterozoico en xeral[7][8]). Para producir colesterol cómpre oxíxeno molecular;[9] así, a presenza do colestano suxire a presenza dalgunha traza de oxíxeno no paleoambiente. O colestano non deriva exclusivamente da diaxénese de moléculas esteroides derivadas de animais; o colestano pode estar tamén asociado coa presenza de, por exemplo, rodófitas e embriófitas,[10][5] se ben a abundancia dese colestano non procedente de metazoos é descoñecida. Os embriófitos producen xeralmente unha variedade de esterois, que se coñecen colectivamente como fitosterois,[11] e o colesterol permanece como un compoñente menor. Ao contrario, as bacterias producen outros triterpenoides cíclicos como os hopanoides e os seus produtos diaxenéticos, os hopanos, utilízanse como biomarcadores bacterianos.
Preservación natural en fósiles
[editar | editar a fonte]
O colesterol ten 256 estereoisómeros, pero só un deles se forma naturalmente durante a produción do colesterol (3β-ol, 5α (H), 14α (H), 17α (H), 20R) e é, polo tanto, o estereoisómero primario que interesa para a medida do colestano. As desviacións desta estereoquímica a miúdo reflicten a diaxénese, a maduración térmica e o nesgo de preservación.
A diaxénese causa normalmente a perda de grupos funcionais e de dobres enlaces nas moléculas orgánicas. No caso concreto do colestano, a diaxénese do colesterol a colestano produce unha molécula que está completamente saturada comparada coa súa contraparte esteroide. Este proceso ocorre sen a perda ou ganancia de átomos de carbono e, polo tanto, pode servir como indicador do esteroide orixinal producido polo organismo no ambiente.[12]
A alteración térmica pode tamén causar a perda da cadea lateral alcano no C17.[13] Un experimento demostrou que despois dunhas 4 semanas a 300 °C, o colestano sofre un 17 % de descomposición da súa cadea lateral alcano. En contraste con isto, a estrutura policíclica (C1-17) é moi estable termicamente. Os procesos diaxenéticos poden tamén causar cambios de posición dos metilos e aromatización.
Alteración estereoquímica
[editar | editar a fonte]Os procesos diaxenéticos adicionais poden alterar aínda máis a molécula de colestano. Por exemplo, o colestano é susceptible a cambios estereoquímicos co paso do tempo a partir do seu isómero natural. Estes cambios poden ser o efecto da alteración térmica ou microbiana. A alteración térmica pode causar cambios na estereoquímica tanto no C20 do centro quiral, coma nos átomos de hidróxeno. A razón de estereoisómeros R/S indícase normalmente como medida da “madureza térmica”.[14] Ao contrario, a conversión do átomo de hidróxeno no C5 da configuración α á β reflicte a actividade microbiana anaerobia,[3] e pode comprenderse por medio de experimentos de marcaxe de isótopos en experimentos controlados con microbios que metabolizan o esteroide de interese.[15][16] Un estudo demostrou que hai dúas reaccións que poden producir unha perda do dobre enlace do colesterol, que son: (1) redución directa do dobre enlace, ou (2) produción dunha cetona antes da redución do dobre enlace, e ambas teñen como resultado unha isomerización do átomo de hidróxeno na posición C5.[15] Os átomos de hidróxeno en C14 e C17α son máis estables e sofren cambios á configuración β moito menos frecuentes que no hidróxeno de C5.
Biomarcadores dos primeiros devanceiros dos animais
[editar | editar a fonte]
A presenza de colestano non indica necesariamente a presenza de animais, mais utilízase a miúdo xunto con outros biomarcadores para indicar a aparición de certos taxons no rexistro fósil; con respecto a isto, un estudo mediu a abundancia relativa de colestano comparado coa doutros biomarcadores triterpenoides para demostrar a aparición das algas durante o Neoproterozoico.[7][17]
Con todo, rastrear as verdadeiras orixes do colestano no rexistro fósil é todo un reto, xa que a maioría das rochas dese período de tempo sufriron un forte metamorfismo, razón pola cal os posibles biomarcadores foron en parte alterados termicamente.[Cómpre referencia] Un estudo ligou a fonte do colestano atopado cun determinado fósil do Ediacárico chamado Dickinsonia, o que axudou á clasificación taxonómica da biota de Ediacara, a cal foi o preludio evolutivo da vida animal.[3] Porén, o colestano non é un marcador específico para os animais e atópase na maioría das liñaxes eucariotas.
Técnicas de medida
[editar | editar a fonte]GC/MS
[editar | editar a fonte]
O colestano pode extraerse de mostras e medirse por GC/MS para cuantificar a abundancia relativa doutros compostos orgánicos. Esta medida faise por extracción dos esteranos nun solvente non polar (por exemplo, diclorometano ou cloroformo) e purificalos nunha fracción de “saturados” usando cromatografía de gases en columna de xel. Os isómeros do colestano elúen da columna segundo o seu peso molecular e a súa diversa estereoquímica, o cal fai que realizar a espectrometría de masas tradicional sexa complicado debido a co-elución dos isómeros. Alternativamente, pódese medir o colestano usando experimentos GC/MS/MS que analizan o fragmento m/z 217 (do ión molecular 372). Este método específico busca primeiro o ión molecular 372 do colestano, e despois fragmenta ese ión molecular ata o seu fragmento m/z 217 para mellorar a identificación de isómeros específicos.
Proporcións do isótopo δ13C
[editar | editar a fonte]Os valores de δ13C do colestano reflicten a composiión en isótopos de carbono dos animais que crearon as moléculas de colesterol orixinais. A composición en isótpos de carbono dos animais crese que está en función da súa dieta;[18] polo tanto, a composición en isótopos de carbono do colestano reflectiría tamén este valor da dieta orixinal. Os valores de δ13C poden medirse usando cromatografía de gas acoplada con IRMS.
Máis en xeral, os esteranos poden utilizarse como indicador de cambios ambientais. Un estudo presentou valores de δ13C de esteranos fronte a hopanos e utilizounos para propoñer cambios na zona fótica no decurso do Mioceno, xa que os cambios no valor isotópico deber ser o resultado de carbono inorgánico disolto na auga ou ben de fraccionamento isotópico biolóxico.[14]
Notas
[editar | editar a fonte]- ↑ The Nomenclature of Steroids Arquivado 2011-05-14 en Wayback Machine., IUPAC
- ↑ Peters, Kenneth E. (Kenneth Eric), 1950- (2007). The biomarker guide. Cambridge University Press. ISBN 9780521039987. OCLC 1015511618.
- ↑ 3,0 3,1 3,2 3,3 3,4 Bobrovskiy, Ilya; Hope, Janet M.; Ivantsov, Andrey; Nettersheim, Benjamin J.; Hallmann, Christian; Brocks, Jochen J. (2018-09-20). "Ancient steroids establish the Ediacaran fossil Dickinsonia as one of the earliest animals". Science 361 (6408): 1246–1249. Bibcode:2018Sci...361.1246B. ISSN 0036-8075. PMID 30237355. doi:10.1126/science.aat7228. hdl:1885/230014.
- ↑ Combaut, Georges; Saenger, Peter (abril de 1984). "Sterols of the amansieae (rhodomelaceae: Rhodophyta)". Phytochemistry 23 (4): 781–782. Bibcode:1984PChem..23..781C. ISSN 0031-9422. doi:10.1016/s0031-9422(00)85025-6.
- ↑ 5,0 5,1 Sonawane, Prashant D.; Pollier, Jacob; Panda, Sayantan; Szymanski, Jedrzej; Massalha, Hassan; Yona, Meital; Unger, Tamar; Malitsky, Sergey; Arendt, Philipp; Pauwels, Laurens; Almekias-Siegl, Efrat (2016-12-22). "Plant cholesterol biosynthetic pathway overlaps with phytosterol metabolism". Nature Plants (en inglés) 3 (1): 16205. ISSN 2055-0278. PMID 28005066. doi:10.1038/nplants.2016.205.
- ↑ Life : the science of biology. Sadava, David E. (9ª ed.). Sunderland, Mass.: Sinauer Associates. 2011. ISBN 978-1429219624. OCLC 368046231.
- ↑ 7,0 7,1 Brocks, Jochen J.; Jarrett, Amber J. M.; Sirantoine, Eva; Hallmann, Christian; Hoshino, Yosuke; Liyanage, Tharika (agosto de 2017). "The rise of algae in Cryogenian oceans and the emergence of animals". Nature 548 (7669): 578–581. Bibcode:2017Natur.548..578B. ISSN 0028-0836. PMID 28813409. doi:10.1038/nature23457.
- ↑ Summons, Roger E; Brassell, Simon C; Eglinton, Geoffrey; Evans, Evan; Horodyski, Robert J; Robinson, Neil; Ward, David M (novembro de 1988). "Distinctive hydrocarbon biomarkers from fossiliferous sediment of the Late Proterozoic Walcott Member, Chuar Group, Grand Canyon, Arizona". Geochimica et Cosmochimica Acta 52 (11): 2625–2637. Bibcode:1988GeCoA..52.2625S. ISSN 0016-7037. doi:10.1016/0016-7037(88)90031-2.
- ↑ Mehta, Sweety (2013-09-17). "Biosynthesis and Regulation of Cholesterol (with Animation) | Animations". PharmaXChange.info. Consultado o 2019-06-04.
- ↑ Summons, Roger E.; Erwin, Douglas H. (2018-09-20). "Chemical clues to the earliest animal fossils". Science 361 (6408): 1198–1199. Bibcode:2018Sci...361.1198S. ISSN 0036-8075. PMID 30237342. doi:10.1126/science.aau9710. hdl:1721.1/134716.2.
- ↑ Darnet, Sylvain; Blary, Aurélien; Chevalier, Quentin; Schaller, Hubert (2021). "Phytosterol Profiles, Genomes and Enzymes – An Overview". Frontiers in Plant Science 12: 878. ISSN 1664-462X. PMC 8172173. PMID 34093623. doi:10.3389/fpls.2021.665206.
- ↑ Grantham, P.J.; Wakefield, L.L. (xaneiro de 1988). "Variations in the sterane carbon number distributions of marine source rock derived crude oils through geological time". Organic Geochemistry 12 (1): 61–73. Bibcode:1988OrGeo..12...61G. ISSN 0146-6380. doi:10.1016/0146-6380(88)90115-5.
- ↑ Mango, Frank D. (xaneiro de 1990). "The origin of light cycloalkanes in petroleum". Geochimica et Cosmochimica Acta 54 (1): 23–27. Bibcode:1990GeCoA..54...23M. ISSN 0016-7037. doi:10.1016/0016-7037(90)90191-m.
- ↑ 14,0 14,1 Schoell, M.; Schouten, S.; Damste, J. S. S.; de Leeuw, J. W.; Summons, R. E. (1994-02-25). "A Molecular Organic Carbon Isotope Record of Miocene Climate Changes". Science 263 (5150): 1122–1125. Bibcode:1994Sci...263.1122S. ISSN 0036-8075. PMID 17831625. doi:10.1126/science.263.5150.1122. hdl:1874/4185.
- ↑ 15,0 15,1 Mermoud, F.; Wünsche, L.; Clerc, O.; Gülaçar, F.O.; Buchs, A. (xaneiro de 1984). "Steroidal ketones in the early diagenetic transformations of Δ5 sterols in different types of sediments". Organic Geochemistry 6: 25–29. ISSN 0146-6380. doi:10.1016/0146-6380(84)90023-8.
- ↑ Taylor, Craig D.; Smith, Steven O.; Gagosian, Robert B. (novembro de 1981). "Use of microbial enrichments for the study of the anaerobic degradation of cholesterol". Geochimica et Cosmochimica Acta 45 (11): 2161–2168. Bibcode:1981GeCoA..45.2161T. ISSN 0016-7037. doi:10.1016/0016-7037(81)90068-5.
- ↑ Hoshino, Yosuke; Poshibaeva, Aleksandra; Meredith, William; Snape, Colin; Poshibaev, Vladimir; Versteegh, Gerard J. M.; Kuznetsov, Nikolay; Leider, Arne; van Maldegem, Lennart; Neumann, Mareike; Naeher, Sebastian (2017). "Cryogenian evolution of stigmasteroid biosynthesis". Science Advances 3 (9): e1700887. Bibcode:2017SciA....3E0887H. PMC 5606710. PMID 28948220. doi:10.1126/sciadv.1700887.
- ↑ Hayes, John M. (2001-12-31). "3. Fractionation of Carbon and Hydrogen Isotopes in Biosynthetic Processes". Stable Isotope Geochemistry. De Gruyter. pp. 225–278. ISBN 9781501508745. doi:10.1515/9781501508745-006.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- Cholestanes Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
