Polyomaviridae
| Polyomaviridae | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Micrografía que mostra unha célula infectada por un poliomavirus (célula grande azul na parte central inferior esquerda). Espécime dunha citroloxía de urina. | |||||||||||||
| Clasificación científica | |||||||||||||
| |||||||||||||
| Xéneros | |||||||||||||
Polyomaviridae é unha familia de virus cuxos hóspedes naturais son principalmente mamíferos e aves, que se adoitan denominar poliomavirus.[1][2] En 2019 recoñecíanse nesta familia catro xéneros e 102 especies, nove das cales non están asignadas a ningún xénero.[3] Catorce destas especies poden infectar seres humanos, mentres que outras, como o SV40 (Simian Virus 40), foron identificados en humanos en menor medida.[4][5] A maioría destes virus son moi comúns e tipicamente asintomáticos na maioría das poboacións humanas estudadas.[6][7] O virus BK está asociado con nefropatías en pacientes de transplantes renais e en transplantes de órganos sólidos non renais,[8][9] o virus JC con leucoencefalopatía multifocal progresiva,[10] e o virus de célula de Merkel con cancro de célula de Merkel.[11]
Estrutura e xenoma
[editar | editar a fonte]
Os poliomavirus son virus de ADN bicatenario con envoltura cun xenoma circular de aproximadamente 5 000 pares de bases. O xenoma está empaquetado dentro dunha cápside viral duns 40-50 nanómetros de diámetro, que ten forma icosaédcrica (simetría T=7).[2][12] A cápside está composta por 72 capsómeros pentaméricos dunha proteína chamada VP1, que pode autoensamblarse formando un icosaedro pechado;[13] de modo que cada pentámero de VP1 está asociado cunha molécula dunha soa das outras dúas proteínas da cápside, chamadas VP2 e VP3.[5]

O xenoma dun poliomavirus típico codifica entre 5 e 9 proteínas, e está dividido en dúas rexións transcricionais chamadas rexións temperá e tardía debido ao momento durante a infección en que se transcriben. Cada rexión é transcrita pola ARN polimerase II da célula hóspede como un só pre-ARNm que contén múltiples xenes. A rexión temperá xeralmente codifica dúas proteínas, os antíxenos tumorais pequeno e grande, producidos por empalme alternativo. A rexión tardía contén as tres proteínas estruturais da cápside, VP1, VP2 e VP3, producidas utilizando sitios alternativos de comezo da tradución. Outros xenes adicionais e outras variacións deste esquema poden verse nalgúns virus: por exemplo, os poliomavirus de roedores teñen unha terceira proteína chamada antíxeno tumoral mediano na rexión temperá, que é extremadamente eficiente en inducir a transformación celular; o SV40 ten unha proteína da cápside adicional, a VP4; nalgúns exemplos os virus teñen proteínas regulatorias adicionais chamadas agnoproteínas expresadas a partir da rexión tardía. O xenoma tamén contén unha rexión regulatoria ou de control non codificante que contén os promotores das rexións temperás e tardías, sitios de comezo da transcrición e a orixe de replicación.[2][12][5][15]
| Virus | Estrutura | Simetría | Cápside | Arranxo xenómico | Segmentación xenómica |
|---|---|---|---|---|---|
| Poliomavirus | Icosaédrica | T=7 | Non envolto | Circular | Monopartito |
Replicación e ciclo vital
[editar | editar a fonte]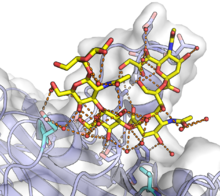
O ciclo vital dos poliomavirus empeza coa súa entrada na célula hóspede. Os receptores celulares para os poliomavirus son residuos de ácidos siálicos de glicanos, normalmente gangliósidos. A adhesión dos poliomavirus ás células hóspede depende da unión da VP1 a glicanos sialilados da superficie celular.[2][12][15][16] En certos virus ocorren interaccións adicionais na superficie celular; por exemplo, o virus JC crese que debe interaccionar co receptor 5HT2A e o virus de célula de Merkel co heparán sulfato.[15][17] Porén, en xeral as interaccións virus-célula están mediadas por moléculas comúns da superficie celular, e, por tanto, probablemente non son un contribuínte importante do tropismo de tipo celular observado en cada virus.[15] Despois de unirse a moléculas da superficie celular, o virión é endocitado e entra no retículo endoplásmico (un comportamento único entre os virus non envoltos coñecidos),[18] onde a estrutura da cápside viral probablemente se ve alterada pola acción dos encimas disulfuro isomerases da célula hóspede.[2][12][19]
Os detalles do tránsito ao núcleo non están claros e poden variar entre distintos poliomavirus. Informouse frecuentemente que unha parcula de virión intacta, aínda que distorsionada, pasa desde o retículo endoplasmático ao citoplasma, onde o xenoma se libera da cápside, posiblemente debido á concentración baixa de calcio no citoplasma.[18] Tanto a expresión dos xenes virais coma a replicación do xenoma viral teñen lugar no núcleo da célula usando a maquinaria do hóspede. Os xenes tenperáns (que comprenden como mínimo o antíxeno tumoral pequeno (ST) e o antíxeno tumoral grande (LT)) exprésanse primeiro, a partir dunha febra monocatenaria de ARN mensaxeiro orixinada por empalme alternativo. Estas proteínas serven para manipular o ciclo celular da célula hóspede, o que desregula a transición da fase G1 á fase S, cando se replica o xenoma da célula hóspede, porque a maquinaria de replicación do ADN da célula hóspede é necesaria para a replicación do xenoma viral.[2][12][15] O mecanismo preciso desta desregulación depende do virus; por exemplo, o antíxeno tumoral grande (LT) do SV40 pode unirse directamente ao p53 da célula hóspede, pero o LT do poliomavirus murino non.[20] O LT induce a replicación do ADN a partir da rexión de control non codificante (NCR) do xenoma viral, despois do cal redúcese a expresión do ARNm temperán e empeza a expresión do ARNm tardío, que codifica as proteínas da cápside viral.[19] A medida que empezan estas interaccións, os LTs pertencentes a varios poliomavirus, incluíndo o poliomavirus de célula de Merkel, presentan un potencial oncoxénico.[21] Describíronse varios mecanismos para regular a transición desde a expresión de xenes temperáns á dos tardíos, como a implicación da proteína LT na represión do promotor temperán,[19] a expresión duns ARNm tardíos non terminados con extensións complementarias aos ARNm temperáns,[15] e a expresión de microARNs regulatorios.[15] A expresión de xenes tardíos ten como resultado a acumulación de proteínas da cápside viral no citoplasma da célula hóspede. Os compoñentes da cápside entran no núcleo para encapsidar novo ADN xenómico viral. Os novos virións poden ensamblarse en factorías virais.[2][12] O mecanismo da liberación viral da célula hóspede varía segundo o poliomavirus; algúns expresan proteínas que facilitan a saída da célula, como a agnoproteína ou a VP4.[19] Nalgúns casos, os altos niveis de virus encapsulados causan a lise da célula, liberándose os virións.[15]
| Virus | Detalles do hóspede | Tropismo de tecido | Detalles da entrada | Detalles da saída | Sitio de replicación | Sitio de ensamblaxe | Transmisión |
|---|---|---|---|---|---|---|---|
| Poliomavirus | Mamíferos; aves | Sistema respiratorio; riles, cerebro | Endocitose de receptor celular | Lise | Núcleo | Núcleo | Oral-fecal |
Proteínas virais
[editar | editar a fonte]Antíxenos tumorais (T)
[editar | editar a fonte]O antíxeno tumoral grande xoga un papel clave na regulación do ciclo de vida viral ao unirse á orixe viral da replicación do ADN, onde promove a síntese de ADN. Ademais, como os poliomavirus dependen da maquinaria da célula hóspede para replicarse, a célula hóspede debe estar en fase S para que esta empece. Debido a isto, o antíxeno T grande tamén modula vías de sinalización celular para estimular a progresión do ciclo celular ao unirse a varias proteínas de control celulares.[22] Isto conséguese por un ataque a dúas bandas ao inhibir os xenes p53 supresores de tumores e a membros da familia do retinoblastoma (pRB),[23] e estimular as vías de crecemento ao unirse ao ADN celular, á ATPase-helicase, á asociación da ADN polimerase α, e unirse a factores do complexo de preiniciación da transcrición.[24] Esta estimulación anormal do ciclo celular é unha forza poderosa para a transformación oncoxénica.
A proteína do antíxeno tumoral pequeno tamén pode activar varias vías celulares que estimulan a proliferación celular. Os antíxenos T pequenos dos poliomavirus teñen como diana a proteína fosfatase 2A (PP2A),[25] un regulador de multisubunidades clave de moitas vías como a Akt, a vía da proteín quinase activada por mitóxeno (MAPK), e a vía da proteína quinase activada polo estrés (SAPK).[26][27] O antíxeno T pequeno do poliomavirus de célula de Merkel codifica un dominio único, chamado dominio de estabilización do LT (LSD), que se une e inhibe a ligase E3 FBXW7 regulando oncoproteínas celulares e virais.[28] A diferenza do SV40, o antíxeno T pequeno do MCV transforma directamente células de roedores in vitro.[29]
O antíxeno tumoral mediano utilízase en organismos modelo desenvolvidos para estudar o cancro, como o sistema MMTV-PyMT, no que o T mediano está acoplado ao promotor de MMTV. Alí, funciona como un oncoxene, mentres que o tecido no que se desenvolve o tumor está determinado polo promotor de MMTV.
Proteínas da cápside
[editar | editar a fonte]A cápside dos poliomavirus consta dun compoñente principal, a proteína da cápside maior VP1, e un ou dous compoñentes menores, proteínas da cápside menores VP2 e VP3. Os pentámeros de VP1 forman a cápside viral icosaédrica pechada e no interior da cápside cada pentámero está asociado cunha molécula ou ben de VP2 ou ben de VP3.[5][30] Algúns poliomavirus, como o poliomavirus de célula de Merkel, non codifican ou expresan a VP3.[31] As proteínas da cápside exprésanse a partir da rexión tardía do xenoma.[5]
Agnoproteína
[editar | editar a fonte]A agnoproteína é unha pequena fosfoproteína multifuncional que se encontra na parte codificante tardía do xenoma dalgúns poliomavirus, especialmente no virus BK, virus JC e SV40. É esencial para a proliferación nos virus que a expresan e pénsase que está implicada na regulación do ciclo vital do virus, concretamente na replicación e saída dos virus da célula hóspede, mais non se coñece o mecanismo exacto.[32][33]
Taxonomía
[editar | editar a fonte]Os poliomavirus son membros do tradicional grupo I de virus (virus de ADN bicatenario). Na clasificación dos poliomavirus fixéronse varias propostas de revisións conforme se descubrían novos membros do grupo. Anteriormente, os poliomavirus e papilomavirus, que comparten moitas características estruturais pero teñen organizacións xenómicas moi diferentes, estaban clasificados xuntos na familia, agora obsoleta, dos Papovaviridae.[34] (O nome Papovaviridae deriva de tres abreviaturas: Pa por Papillomavirus, Po por Polyomavirus e Va por "vacuolantes.")[35] Os poliomaviruses foron divididos en tres grandes clados (é dicir, grupos relacionados xeneticamente): o clado SV40, o clado aviario e o clado do poliomavirus murino.[36] Unha posterior reclasificación proposta polo Comité Internacional de Taxonomía de Virus (ICTV) recomendou dividir a familia Polyomaviridae en tres xéneros:[37]
- Xénero Orthopolyomavirus (especie tipo SV40)
- Xénero Wukipolyomavirus (especie tipo poliomavirus KI)
- Xénero Avipolyomavirus (especie tipo poliomavirua aviar)
Non obstante, o actual sistema de clasificación do ICTV recoñece catro xénenros e 102 especies, das cales nove non puideron asignarse a ningún xénero. Este sistema mantén a distinción entre os virus aviarios e os mamalianos, agrupando o subconxunto aviario no xénero Gammapolyomavirus.[3]
- Xénero Alphapolyomavirus, especie tipo Mus musculus polyomavirus 1 (poliomavirus murino)
- Xénero Betapolyomavirus, especie tipo Macaca mulatta polyomavirus 1 (SV40)
- Xénero Deltapolyomavirus, especie tipo Human polyomavirus 6
- Xénero Gammapolyomavirus, especie tipo Aves polyomavirus 1
As seguintes especies non foron asignadas a ningún xéenro:[3]
- Ailuropoda melanoleuca polyomavirus 1
- Bos taurus polyomavirus 1
- Centropristis striata polyomavirus 1
- Delphinus delphis polyomavirus 1
- Procyon lotor polyomavirus 2
- Rhynchobatus djiddensis polyomavirus 1
- Sparus aurata polyomavirus 1
- Trematomus bernacchii polyomavirus 1
- Trematomus pennellii polyomavirus 1
A descrición de novos virus deste grupo segue en marcha. Entre os novos están o poliomavirus da londra mariña 1[38] e o poliomavirus da alpaca.[39] Outro virus é o poliomavirus do panda xigante 1.[40] Outro virus foi descrito nos roedores sigmodontinos.[41] Outro foi descrito nas tupaias.[42]
Poliomavirus humanos
[editar | editar a fonte]A maioría dos poliomavirus non infectan a humanos. Dos poliomavirus que estaban catalogados en 2017, só se coñecía un total de 14 que tivesen como hóspede o ser humano.[4] Porén, algúns poliomavirus están asociados con enfermidades humanas, especialmente en individuos inmunocomprometidos. O MCV é moi diverxente respecto doutros poliomavirus humanos e está máis estreitamente relacionado co poliomavirus murino. O poliomavirus asociado a Trichodysplasia spinulosa (TSV) está distantemente relacionado co MCV. Dous virus, o HPyV6 e o HPyV7, están máis estreitamente relacionados cos virus KI e WU, mentres que o HPyV9 está máis próximo ao poliomavirus linfotrópico derivado do mono verde africano (LPV).
Describíronse catorce destes virus patóxenos humanos.[43] O poliomavirus Lyon IARC está relacionado co poliomavirus de mapache.
Lista dos poliomavirus humanos
[editar | editar a fonte]En 2017 identificáranse os seguintes 14 poliomavirus que teñen como hóspede os humanos e o seu xenoma foi secuenciado:[4]
| Especie | Xénero proposto | Nome do virus | Abreviatura | NCBI RefSeq | Ano de descubrimento | Correlato clínico (se hai) | Referencias |
|---|---|---|---|---|---|---|---|
| Human polyomavirus 5 | Alfa | poliomavirus de célula de Merkel | MCPyV | NC_010277 | 2008 | Cancro de célula de Merkel[5] | [44][11][45] |
| Human polyomavirus 8 | Alfa | poliomavirus de Trichodysplasia spinulosa | TSPyV | NC_014361 | 2010 | Trichodysplasia spinulosa[5] | [46][47] |
| Human polyomavirus 9 | Alfa | poliomavirus humano 9 | HPyV9 | NC_015150 | 2011 | Ningún coñecido | [48] |
| Human polyomavirus 12 | Alfa | poliomavirus humano 12 | HPyV12 | NC_020890 | 2013 | Ningún coñecido | [49] |
| Human polyomavirus 13 | Alfa | poliomavirus de New Jersey | NJPyV | NC_024118 | 2014 | Ningún coñecido | [50] |
| Human polyomavirus 1 | Beta | poliomavirus BK | BKPyV | NC_001538 | 1971 | Nefropatía asociada a poliomavirus; cistite hemorráxica[5] | [51] |
| Human polyomavirus 2 | Beta | poliomavirus JC | JCPyV | NC_001699 | 1971 | Leucoencefalopatía multifocal progresiva[5] | [52] |
| Human polyomavirus 3 | Beta | poliomavirus KI | KIPyV | NC_009238 | 2007 | Ningún coñecido | [53] |
| Human polyomavirus 4 | Beta | poliomavirus WU | WUPyV | NC_009539 | 2007 | Ningún coñecido | [14] |
| Human polyomavirus 6 | Delta | poliomavirus humano 6 | HPyV6 | NC_014406 | 2010 | Dermatose disqueratótica e prurítica asociada a HPyV6 (H6PD)[54] | [31] |
| Human polyomavirus 7 | Delta | poliomavirus humano 7 | HPyV7 | NC_014407 | 2010 | Hiperplasia epitelial relacionada con HPyV7[54][55][56] | [31] |
| Human polyomavirus 10 | Delta | poliomavirus MW | MWPyV | NC_018102 | 2012 | Ningún coñecido | [57][58][59] |
| Human polyomavirus 11 | Delta | poliomavirus STL | STLPyV | NC_020106 | 2013 | Ningún coñecido | [60] |
| Human polyomavirus 14 | Alfa | poliomavirus Lyon IARC | LIPyV | NC_034253.1 | 2017 | Ningún coñecido | [61][62] |
O Deltapolyomavirus contén só os catro virus humanos mostrados na táboa, dos que o poliomavirus humano 6 é a especie tipo. Os grupos Alfa e Beta conteñen virus que infectan diversos mamíferos. O grupo Gamma comprende os virus aviarios.[4] Clinicamente as asociacións con enfermidades significativas só se mostran onde se espera causalidade.[5][63]
En humanos detectáronse anticorpos para o poliomavirus linfotrópico de mono, o que suxire que este virus (ou un virus estreitamente relacionado) podería infectar humanos.[64]
Importancia clínica
[editar | editar a fonte]Todos os poliomavirus causan infeccións moi comúns na infancia e mocidade.[65] A maioría destas infeccións parecen causar poucos ou ningúns síntomas. Estes virus probablemente persisten durante toda a vida en case todos os adultos. As enfermidades causadas polas infeccións por poliomavirus humanos son máis comúns en persoas inmunocomprometidas; entre as asociacións con enfermidades están o virus BK coa nefropatía en pacientes de transplante renal e de transplante de órgano sólido non renal,[8][9] o virus JC coa leucoencefalopatía multifocal progresiva,[10] e o virus de célula de Merkel (MCV) co cancro de célula de Merkel.[11]
SV40
[editar | editar a fonte]O SV40 replícase nos riles de monos sen causar enfermidade, pero pode causar cancro en roedaores en condicións de laboratorio. Nas décadas de 1950 e inicios da de 1960, unhas 100 millóns de persoas puideron ser expostas ao SV40 debido a unha contaminación non detectada previamente por SV40 da vacina da polio, o que creou preocupación sobre se este virus podería causar enfermidade en humanos.[66][67] Aínda que se informou que estaba presente nalgúns cancros humanos, como en tumors cerebrais, tumores óseos, mesoteliomas e linfomas non de Hodgkin,[68] a súa detección precisa é a miúdo confundida cos altos niveis de reactividade cruzada entre o SV40 e poliomavirus humanos moi espallados.[67] A maioría dos virólogos descartan o SV40 como causa de cancros humanos.[66][69][70]
Diagnose
[editar | editar a fonte]A diagnose dos poliomavirus case sempre ocorre despois da infección primaria, xa que é asintomática ou subclínica. As probas de anticorpos son as que se utilizan comunemente para detectar a presenza de anticorpos contra algúns destes virus.[71] Frecuentemente cómpre facer ensaios de competición para distinguir entre poliomavirus moi semellantes.[72]
En casos de leucoencefalopatía multifocal progresiva, utilízase un anticorpo para o antíxeno T de SV40 con reactividade cruzada (normalemnte o Pab419) para marcar os tecidos directamente para a presenza do antíxeno T do virus JC. Pode usarse a PCR en biopsias de tecidos ou de líquido cefalorraquídeo para amplificar o ADN de poliomavirus. Isto non só permite a detección de poliomavirus senón tamén dicir que subtipo é.[73]
Hai tres técnicas de diagnóstico principais que se usan para a diagnose da reactivación de poliomavirus na nefropatía por poliomavirus: a citoloxía de urina, a cuantificación da carga viral en urina e sangue, e a biopsia renal.[71] A reactivación de poliomavirus nos riles e tracto urinario causa o vertido de células infectads, virións e proteínas virais na urina. Isto permite nas citoloxías de urina examinar estas células, que se teñen inclusións de poliomavirus no núcleo, serven como diagnóstico de infección.[74] Ademais, como a urina das persoas infectadas contén virións ou ADN viral, pode facerse a cuantificación da carga viral por PCR.[75] Isto tamén é válido para o sangue.
Pode utilizarse tamén a biopsia renal se os dous métodos anteriores non son concluíntes ou se se quere estimar a carga viral específica no tecido renal. Igual que na citoloxía de urina, as células renais son examinadas con microscopio óptico para buscar inclusións de poliomavirus no núcleo, así como a lise e partes virais no fluído extracelular. A carga viral mídese, igual que antes, por PCR.[Cómpre referencia]
A tinguidura de tecidos usando un anticorpo monoclonal contra o antíxeno T do MCV é útil para diferenciar o carcinoma de célula de Merkel doutros tumores de células pequenas redondas.[76] Desenvolvéronse tests sanguíneos para detectar anticorpos para o MCV e mostran que a infección polo virus está moi espallada aínda que os pacientes con carcinoma de célula de Merkel teñen respostas de anticorpos excepcionalmente máis altas que as persoas infectadas asintomaticamente.[7][77][78][79]
Uso para rastrear as migracións humanas
[editar | editar a fonte]O virus JC parece ser un prometedor marcador xenético para estudar as migracións e evolución humanas.[80] Este virus pórtano entre o 70 e o 90 % dos humanos e xeralmente é transmitido de pais a fillos. Porén, este método non parece ser fiable para rastrear a orixe africana recente dos humanos modernos.
Historia
[editar | editar a fonte]O poliomavirus murino foi o primeiro poliomavirus que se descubriu, grazas a Ludwik Gross en 1953, que informou del como un extracto de leucemia de rato con capacidade de inducir tumores de glándula parótide.[81] O axente causante foi identificado como virus por Sarah Stewart e Bernice Eddy, e en honra delas foi denominado durante un tempo "polioma SE", coas súas iniciais.[82][83][84] O termo "polioma" refírese á capacidade do virus de producir múltiples (poli-) tumores (-oma) en certas condicións. O nome foi despois criticado por ser como un "sándwich lingüístico sen carne" ("sen carne" porque anbos os morfemas no termo "polioma" son afixos e non hai lexemas) que daba pouca información sobre a bioloxía do virus; de feito, investigacións posteriores atoparon que a maioría dos poliomaviruses raramente causan enfermidades clinicamente significativas nos seus organismos hóspedces en condicións naturais.[85]
En 2017 identificáranse e secuenciáranse ducias de poliomavirus, que infectan principalmente aves e mamíferos. Coñécense dous poliomavirus que infectan peixes das especies Centropristis striata (un serránido)[86] e Sparus aurata (a dourada).[87] Coñécense un total de 14 poliomavirus que infectan humanos.[4]
Notas
[editar | editar a fonte]- ↑ Moens U, Calvignac-Spencer S, Lauber C, Ramqvist T, Feltkamp MC, Daugherty MD, Verschoor EJ, Ehlers B (June 2017). "ICTV Virus Taxonomy Profile: Polyomaviridae". The Journal of General Virology 98 (6): 1159–1160. PMC 5656788. PMID 28640744. doi:10.1099/jgv.0.000839.
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 "ICTV Report Polyomaviridae".
- ↑ 3,0 3,1 3,2 "Virus Taxonomy: 2019 Release". talk.ictvonline.org. International Committee on Taxonomy of Viruses. Arquivado dende o orixinal o 20 de marzo de 2020. Consultado o 26 April 2020.
- ↑ 4,0 4,1 4,2 4,3 4,4 Calvignac-Spencer S, Feltkamp MC, Daugherty MD, Moens U, Ramqvist T, Johne R, Ehlers B (June 2016). "A taxonomy update for the family Polyomaviridae". Archives of Virology 161 (6): 1739–50. PMID 26923930. doi:10.1007/s00705-016-2794-y.
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 DeCaprio JA, Garcea RL (April 2013). "A cornucopia of human polyomaviruses". Nature Reviews. Microbiology 11 (4): 264–76. PMC 3928796. PMID 23474680. doi:10.1038/nrmicro2992.
- ↑ Gossai A, Waterboer T, Nelson HH, Michel A, Willhauck-Fleckenstein M, Farzan SF, Hoen AG, Christensen BC, Kelsey KT, Marsit CJ, Pawlita M, Karagas MR (January 2016). "Seroepidemiology of Human Polyomaviruses in a US Population". American Journal of Epidemiology 183 (1): 61–9. PMC 5006224. PMID 26667254. doi:10.1093/aje/kwv155.
- ↑ 7,0 7,1 Kean JM, Rao S, Wang M, Garcea RL (March 2009). "Seroepidemiology of human polyomaviruses". PLOS Pathogens 5 (3): e1000363. PMC 2655709. PMID 19325891. doi:10.1371/journal.ppat.1000363.
- ↑ 8,0 8,1 Jamboti JS (August 2016). "BK virus nephropathy in renal transplant recipients". Nephrology 21 (8): 647–54. PMID 26780694. doi:10.1111/nep.12728.
- ↑ 9,0 9,1 Kuppachi S, Kaur D, Holanda DG, Thomas CP (April 2016). "BK polyoma virus infection and renal disease in non-renal solid organ transplantation". Clinical Kidney Journal 9 (2): 310–8. PMC 4792618. PMID 26985385. doi:10.1093/ckj/sfv143.
- ↑ 10,0 10,1 Adang L, Berger J (2015). "Progressive Multifocal Leukoencephalopathy". F1000Research 4: 1424. PMC 4754031. PMID 26918152. doi:10.12688/f1000research.7071.1.
- ↑ 11,0 11,1 11,2 Feng H, Shuda M, Chang Y, Moore PS (February 2008). "Clonal integration of a polyomavirus in human Merkel cell carcinoma". Science 319 (5866): 1096–100. Bibcode:2008Sci...319.1096F. PMC 2740911. PMID 18202256. doi:10.1126/science.1152586.
- ↑ Salunke DM, Caspar DL, Garcea RL (September 1986). "Self-assembly of purified polyomavirus capsid protein VP1". Cell 46 (6): 895–904. PMID 3019556. doi:10.1016/0092-8674(86)90071-1.
- ↑ 14,0 14,1 Gaynor AM, Nissen MD, Whiley DM, Mackay IM, Lambert SB, Wu G, Brennan DC, Storch GA, Sloots TP, Wang D (May 2007). "Identification of a novel polyomavirus from patients with acute respiratory tract infections". PLOS Pathogens 3 (5): e64. PMC 1864993. PMID 17480120. doi:10.1371/journal.ppat.0030064.
- ↑ 15,0 15,1 15,2 15,3 15,4 15,5 15,6 15,7 International Agency for Research on Cancer (2013). "Introduction to Polyomaviruses" (PDF). IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 104: 121–131.
- ↑ 16,0 16,1 Buch MH, Liaci AM, O'Hara SD, Garcea RL, Neu U, Stehle T (October 2015). "Structural and Functional Analysis of Murine Polyomavirus Capsid Proteins Establish the Determinants of Ligand Recognition and Pathogenicity". PLOS Pathogens 11 (10): e1005104. PMC 4608799. PMID 26474293. doi:10.1371/journal.ppat.1005104.
- ↑ Schowalter RM, Pastrana DV, Buck CB (July 2011). "Glycosaminoglycans and sialylated glycans sequentially facilitate Merkel cell polyomavirus infectious entry". PLOS Pathogens 7 (7): e1002161. PMC 3145800. PMID 21829355. doi:10.1371/journal.ppat.1002161.
- ↑ 18,0 18,1 Inoue T, Tsai B (January 2013). "How viruses use the endoplasmic reticulum for entry, replication, and assembly". Cold Spring Harbor Perspectives in Biology 5 (1): a013250. PMC 3579393. PMID 23284050. doi:10.1101/cshperspect.a013250.
- ↑ 19,0 19,1 19,2 19,3 Gjoerup O, Chang Y (2010). "Update on human polyomaviruses and cancer". Advances in Cancer Research 106: 1–51. ISBN 9780123747716. PMID 20399955. doi:10.1016/S0065-230X(10)06001-X.
- ↑ Andrabi S, Hwang JH, Choe JK, Roberts TM, Schaffhausen BS (2011). "Comparisons between Murine Polyomavirus and Simian Virus 40 Show Significant Differences in Small T Antigen Function". Journal of Virology 85 (20): 10649–10658. PMC 3187521. PMID 21835797. doi:10.1128/JVI.05034-11.
- ↑ Rotondo JC, Bononi I, Puozzo A, Govoni M, Foschi V, Lanza G, Gafà R, Gaboriaud P, Touzé FA, Selvatici R, Martini F, Tognon M (July 2017). "Merkel Cell Carcinomas Arising in Autoimmune Disease Affected Patients Treated with Biologic Drugs, Including Anti-TNF". Clinical Cancer Research 23 (14): 3929–3934. PMID 28174236. doi:10.1158/1078-0432.CCR-16-2899.
- ↑ White MK, Gordon J, Reiss K, Del Valle L, Croul S, Giordano A, Darbinyan A, Khalili K (December 2005). "Human polyomaviruses and brain tumors". Brain Research. Brain Research Reviews 50 (1): 69–85. PMID 15982744. doi:10.1016/j.brainresrev.2005.04.007.
- ↑ Kazem S, van der Meijden E, Wang RC, Rosenberg AS, Pope E, Benoit T, Fleckman P, Feltkamp MC (2014). "Polyomavirus-associated Trichodysplasia spinulosa involves hyperproliferation, pRB phosphorylation and upregulation of p16 and p21". PLOS One 9 (10): e108947. Bibcode:2014PLoSO...9j8947K. PMC 4188587. PMID 25291363. doi:10.1371/journal.pone.0108947.
- ↑ Kelley WL, Georgopoulos C (April 1997). "The T/t common exon of simian virus 40, JC, and BK polyomavirus T antigens can functionally replace the J-domain of the Escherichia coli DnaJ molecular chaperone". Proceedings of the National Academy of Sciences of the United States of America 94 (8): 3679–84. Bibcode:1997PNAS...94.3679K. PMC 20500. PMID 9108037. doi:10.1073/pnas.94.8.3679.
- ↑ Pallas DC, Shahrik LK, Martin BL, Jaspers S, Miller TB, Brautigan DL, Roberts TM (January 1990). "Polyoma small and middle T antigens and SV40 small t antigen form stable complexes with protein phosphatase 2A". Cell 60 (1): 167–76. PMID 2153055. doi:10.1016/0092-8674(90)90726-u.
- ↑ Sontag E, Fedorov S, Kamibayashi C, Robbins D, Cobb M, Mumby M (December 1993). "The interaction of SV40 small tumor antigen with protein phosphatase 2A stimulates the map kinase pathway and induces cell proliferation". Cell 75 (5): 887–97. PMID 8252625. doi:10.1016/0092-8674(93)90533-V.
- ↑ Watanabe G, Howe A, Lee RJ, Albanese C, Shu IW, Karnezis AN, Zon L, Kyriakis J, Rundell K, Pestell RG (November 1996). "Induction of cyclin D1 by simian virus 40 small tumor antigen". Proceedings of the National Academy of Sciences of the United States of America 93 (23): 12861–6. Bibcode:1996PNAS...9312861W. PMC 24011. PMID 8917510. doi:10.1073/pnas.93.23.12861.
- ↑ Kwun HJ, Shuda M, Feng H, Camacho CJ, Moore PS, Chang Y (August 2013). "Merkel cell polyomavirus small T antigen controls viral replication and oncoprotein expression by targeting the cellular ubiquitin ligase SCFFbw7". Cell Host & Microbe 14 (2): 125–35. PMC 3764649. PMID 23954152. doi:10.1016/j.chom.2013.06.008.
- ↑ Shuda M, Kwun HJ, Feng H, Chang Y, Moore PS (September 2011). "Human Merkel cell polyomavirus small T antigen is an oncoprotein targeting the 4E-BP1 translation regulator". The Journal of Clinical Investigation 121 (9): 3623–34. PMC 3163959. PMID 21841310. doi:10.1172/JCI46323.
- ↑ Chen XS, Stehle T, Harrison SC (June 1998). "Interaction of polyomavirus internal protein VP2 with the major capsid protein VP1 and implications for participation of VP2 in viral entry". The EMBO Journal (en inglés) 17 (12): 3233–40. PMC 1170661. PMID 9628860. doi:10.1093/emboj/17.12.3233.
- ↑ 31,0 31,1 31,2 Schowalter RM, Pastrana DV, Pumphrey KA, Moyer AL, Buck CB (June 2010). "Merkel cell polyomavirus and two previously unknown polyomaviruses are chronically shed from human skin". Cell Host & Microbe 7 (6): 509–15. PMC 2919322. PMID 20542254. doi:10.1016/j.chom.2010.05.006.
- ↑ Sariyer IK, Saribas AS, White MK, Safak M (May 2011). "Infection by agnoprotein-negative mutants of polyomavirus JC and SV40 results in the release of virions that are mostly deficient in DNA content". Virology Journal 8: 255. PMC 3127838. PMID 21609431. doi:10.1186/1743-422X-8-255.
- ↑ Saribas AS, Coric P, Hamazaspyan A, Davis W, Axman R, White MK, Abou-Gharbia M, Childers W, Condra JH, Bouaziz S, Safak M (October 2016). "Emerging From the Unknown: Structural and Functional Features of Agnoprotein of Polyomaviruses". Journal of Cellular Physiology 231 (10): 2115–27. PMC 5217748. PMID 26831433. doi:10.1002/jcp.25329.
- ↑ "ICTV Taxonomy Website". Arquivado dende o orixinal o 20 de marzo de 2020. Consultado o 09 de agosto de 2020.
- ↑ International Agency for Research on Cancer (2013). "IARC Working Group on the Evaluation of Carcinogenic Risk to Humans. Malaria and Some Polyomaviruses (SV40, BK, JC, and Merkel Cell Viruses).". IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 104.
- ↑ Pérez-Losada M, Christensen RG, McClellan DA, Adams BJ, Viscidi RP, Demma JC, Crandall KA (June 2006). "Comparing phylogenetic codivergence between polyomaviruses and their hosts". Journal of Virology 80 (12): 5663–9. PMC 1472594. PMID 16731904. doi:10.1128/JVI.00056-06.
- ↑ Johne R, Buck CB, Allander T, Atwood WJ, Garcea RL, Imperiale MJ, Major EO, Ramqvist T, Norkin LC (September 2011). "Taxonomical developments in the family Polyomaviridae". Archives of Virology 156 (9): 1627–34. PMC 3815707. PMID 21562881. doi:10.1007/s00705-011-1008-x.
- ↑ Siqueira JD, Ng TF, Miller M, Li L, Deng X, Dodd E, Batac F, Delwart E (July 2017). "Endemic infection of stranded southern sea otters (Enhydra lutris nereis) with novel parvovirus, polyomavirus, and adenovirus". Journal of Wildlife Diseases 53 (3): 532–542. PMID 28192039. doi:10.7589/2016-04-082.
- ↑ Dela Cruz FN, Li L, Delwart E, Pesavento PA (2017). "A novel pulmonary polyomavirus in alpacas (Vicugna pacos)". Veterinary Microbiology 201: 49–55. PMID 28284622. doi:10.1016/j.vetmic.2017.01.005.
- ↑ Qi D, Shan T, Liu Z, Deng X, Zhang Z, Bi W, Owens JR, Feng F, Zheng L, Huang F, Delwart E, Hou R, Zhang W (2017). "A novel polyomavirus from the nasal cavity of a giant panda (Ailuropoda melanoleuca)". Virology Journal 14 (1): 207. PMC 5658932. PMID 29078783. doi:10.1186/s12985-017-0867-5.
- ↑ Gonçalves Motta Maia F, Marciel de Souza W, Sabino-Santos G, Jorge Fumagalli M, Modha S, Ramiro Murcia P, Tadeu Moraes Figueiredo L (2018). "A novel polyomavirus in sigmodontine rodents from São Paulo State, Brazil". Archives of Virology 163 (10): 2913–2915. PMID 29931397. doi:10.1007/s00705-018-3913-8.
- ↑ Liu P, Qiu Y, Xing C, Zhou JH, Yang WH, Wang Q, Li JY, Han X, Zhang YZ, Ge XY (2019). "Detection and genome characterization of two novel papillomaviruses and a novel polyomavirus in tree shrew (Tupaia belangeri chinensis) in China". Virol J 16 (1): 35. PMC 6423848. PMID 30885224. doi:10.1186/s12985-019-1141-9.
- ↑ Gheit T, Dutta S, Oliver J, Robitaille A, Hampras S, Combes JD, McKay-Chopin S, Le Calvez-Kelm F, Fenske N, Cherpelis B, Giuliano AR, Franceschi S, McKay J, Rollison DE, Tommasino M (2017). "Isolation and characterization of a novel putative human polyomavirus". Virology 506: 45–54. PMID 28342387. doi:10.1016/j.virol.2017.03.007.
- ↑ Altman LK (2008-01-18). "Virus Is Linked to a Powerful Skin Cancer". The New York Times. Consultado o 2008-01-18.
- ↑ Shuda M, Arora R, Kwun HJ, Feng H, Sarid R, Fernández-Figueras MT, Tolstov Y, Gjoerup O, Mansukhani MM, Swerdlow SH, Chaudhary PM, Kirkwood JM, Nalesnik MA, Kant JA, Weiss LM, Moore PS, Chang Y (September 2009). "Human Merkel cell polyomavirus infection I. MCV T antigen expression in Merkel cell carcinoma, lymphoid tissues and lymphoid tumors". International Journal of Cancer 125 (6): 1243–9. PMC 6388400. PMID 19499546. doi:10.1002/ijc.24510.
- ↑ van der Meijden E, Janssens RW, Lauber C, Bouwes Bavinck JN, Gorbalenya AE, Feltkamp MC (July 2010). "Discovery of a new human polyomavirus associated with trichodysplasia spinulosa in an immunocompromized patient". PLOS Pathogens 6 (7): e1001024. PMC 2912394. PMID 20686659. doi:10.1371/journal.ppat.1001024.
- ↑ Kazem S, van der Meijden E, Feltkamp MC (August 2013). "The trichodysplasia spinulosa-associated polyomavirus: virological background and clinical implications". APMIS 121 (8): 770–82. PMID 23593936. doi:10.1111/apm.12092.
- ↑ Scuda N, Hofmann J, Calvignac-Spencer S, Ruprecht K, Liman P, Kühn J, Hengel H, Ehlers B (May 2011). "A novel human polyomavirus closely related to the african green monkey-derived lymphotropic polyomavirus". Journal of Virology 85 (9): 4586–90. PMC 3126223. PMID 21307194. doi:10.1128/jvi.02602-10.
- ↑ Korup S, Rietscher J, Calvignac-Spencer S, Trusch F, Hofmann J, Moens U, Sauer I, Voigt S, Schmuck R, Ehlers B (2013). "Identification of a novel human polyomavirus in organs of the gastrointestinal tract". PLOS One 8 (3): e58021. Bibcode:2013PLoSO...858021K. PMC 3596337. PMID 23516426. doi:10.1371/journal.pone.0058021.
- ↑ Mishra N, Pereira M, Rhodes RH, An P, Pipas JM, Jain K, Kapoor A, Briese T, Faust PL, Lipkin WI (November 2014). "Identification of a novel polyomavirus in a pancreatic transplant recipient with retinal blindness and vasculitic myopathy". The Journal of Infectious Diseases 210 (10): 1595–9. PMC 4334791. PMID 24795478. doi:10.1093/infdis/jiu250.
- ↑ Gardner SD, Field AM, Coleman DV, Hulme B (June 1971). "New human papovavirus (B.K.) isolated from urine after renal transplantation". Lancet 1 (7712): 1253–7. PMID 4104714. doi:10.1016/s0140-6736(71)91776-4.
- ↑ Padgett BL, Walker DL, ZuRhein GM, Eckroade RJ, Dessel BH (June 1971). "Cultivation of papova-like virus from human brain with progressive multifocal leucoencephalopathy". Lancet 1 (7712): 1257–60. PMID 4104715. doi:10.1016/S0140-6736(71)91777-6.
- ↑ Allander T, Andreasson K, Gupta S, Bjerkner A, Bogdanovic G, Persson MA, Dalianis T, Ramqvist T, Andersson B (April 2007). "Identification of a third human polyomavirus". Journal of Virology 81 (8): 4130–6. PMC 1866148. PMID 17287263. doi:10.1128/JVI.00028-07.
- ↑ 54,0 54,1 Nguyen KD, Lee EE, Yue Y, Stork J, Pock L, North JP, Vandergriff T, Cockerell C, Hosler GA, Pastrana DV, Buck CB, Wang RC (May 2017). "Human polyomavirus 6 and 7 are associated with pruritic and dyskeratotic dermatoses". Journal of the American Academy of Dermatology 76 (5): 932–940.e3. PMC 5392424. PMID 28040372. doi:10.1016/j.jaad.2016.11.035.
- ↑ Ho J, Jedrych JJ, Feng H, Natalie AA, Grandinetti L, Mirvish E, Crespo MM, Yadav D, Fasanella KE, Proksell S, Kuan SF, Pastrana DV, Buck CB, Shuda Y, Moore PS, Chang Y (May 2015). "Human polyomavirus 7-associated pruritic rash and viremia in transplant recipients". The Journal of Infectious Diseases 211 (10): 1560–5. PMC 4425822. PMID 25231015. doi:10.1093/infdis/jiu524.
- ↑ Toptan T, Yousem SA, Ho J, Matsushima Y, Stabile LP, Fernández-Figueras MT, Bhargava R, Ryo A, Moore PS, Chang Y (February 2016). "Survey for human polyomaviruses in cancer". JCI Insight 1 (2). PMC 4811373. PMID 27034991. doi:10.1172/jci.insight.85562.
- ↑ Siebrasse EA, Reyes A, Lim ES, Zhao G, Mkakosya RS, Manary MJ, Gordon JI, Wang D (October 2012). "Identification of MW polyomavirus, a novel polyomavirus in human stool". Journal of Virology 86 (19): 10321–6. PMC 3457274. PMID 22740408. doi:10.1128/JVI.01210-12.
- ↑ Buck CB, Phan GQ, Raiji MT, Murphy PM, McDermott DH, McBride AA (October 2012). "Complete genome sequence of a tenth human polyomavirus". Journal of Virology 86 (19): 10887. PMC 3457262. PMID 22966183. doi:10.1128/JVI.01690-12.
- ↑ Yu G, Greninger AL, Isa P, Phan TG, Martínez MA, de la Luz Sanchez M, Contreras JF, Santos-Preciado JI, Parsonnet J, Miller S, DeRisi JL, Delwart E, Arias CF, Chiu CY (2012). "Discovery of a novel polyomavirus in acute diarrheal samples from children". PLOS One 7 (11): e49449. Bibcode:2012PLoSO...749449Y. PMC 3498111. PMID 23166671. doi:10.1371/journal.pone.0049449.
- ↑ Lim ES, Reyes A, Antonio M, Saha D, Ikumapayi UN, Adeyemi M, Stine OC, Skelton R, Brennan DC, Mkakosya RS, Manary MJ, Gordon JI, Wang D (February 2013). "Discovery of STL polyomavirus, a polyomavirus of ancestral recombinant origin that encodes a unique T antigen by alternative splicing". Virology 436 (2): 295–303. PMC 3693558. PMID 23276405. doi:10.1016/j.virol.2012.12.005.
- ↑ Gheit, Tarik; Dutta, Sankhadeep; Oliver, Javier; Robitaille, Alexis; Hampras, Shalaka; Combes, Jean-Damien; McKay-Chopin, Sandrine; Calvez-Kelm, Florence Le; Fenske, Neil (2017). "Isolation and characterization of a novel putative human polyomavirus". Virology 506: 45–54. PMID 28342387. doi:10.1016/j.virol.2017.03.007.
- ↑ Prado JC, Monezi TA, Amorim AT, Lino V, Paladino A, Boccardo E (2018). "Human polyomaviruses and cancer: an overview". Clinics (Sao Paulo) 73 (suppl 1): e558s. PMC 6157077. PMID 30328951. doi:10.6061/clinics/2018/e558s.
- ↑ Dalianis T, Hirsch HH (March 2013). "Human polyomaviruses in disease and cancer". Virology 437 (2): 63–72. PMID 23357733. doi:10.1016/j.virol.2012.12.015.
- ↑ Van Ghelue M, Khan MT, Ehlers B, Moens U (November 2012). "Genome analysis of the new human polyomaviruses". Reviews in Medical Virology 22 (6): 354–77. PMID 22461085. doi:10.1002/rmv.1711.
- ↑ Egli A, Infanti L, Dumoulin A, Buser A, Samaridis J, Stebler C, Gosert R, Hirsch HH (March 2009). "Prevalence of polyomavirus BK and JC infection and replication in 400 healthy blood donors". The Journal of Infectious Diseases 199 (6): 837–46. PMID 19434930. doi:10.1086/597126.
- ↑ 66,0 66,1 Poulin DL, DeCaprio JA (September 2006). "Is there a role for SV40 in human cancer?". Journal of Clinical Oncology 24 (26): 4356–65. PMID 16963733. doi:10.1200/JCO.2005.03.7101.
- ↑ 67,0 67,1 zur Hausen H (December 2003). "SV40 in human cancers--an endless tale?". International Journal of Cancer 107 (5): 687. PMID 14566815. doi:10.1002/ijc.11517.
- ↑ Gazdar AF, Butel JS, Carbone M (December 2002). "SV40 and human tumours: myth, association or causality?". Nature Reviews. Cancer 2 (12): 957–64. PMID 12459734. doi:10.1038/nrc947.
- ↑ Carroll-Pankhurst C, Engels EA, Strickler HD, Goedert JJ, Wagner J, Mortimer EA (November 2001). "Thirty-five year mortality following receipt of SV40- contaminated polio vaccine during the neonatal period". British Journal of Cancer 85 (9): 1295–7. PMC 2375249. PMID 11720463. doi:10.1054/bjoc.2001.2065.
- ↑ Shah KV (January 2007). "SV40 and human cancer: a review of recent data". International Journal of Cancer 120 (2): 215–23. PMID 17131333. doi:10.1002/ijc.22425.
- ↑ 71,0 71,1 Drachenberg CB, Hirsch HH, Ramos E, Papadimitriou JC (December 2005). "Polyomavirus disease in renal transplantation: review of pathological findings and diagnostic methods". Human Pathology 36 (12): 1245–55. PMID 16311117. doi:10.1016/j.humpath.2005.08.009.
- ↑ Viscidi RP, Clayman B (2006). "Serological Cross Reactivity between Polyomavirus Capsids". En Ahsan N. Polyomaviruses and Human Diseases. Advances in Experimental Medicine and Biology 577. pp. 73–84. ISBN 978-0-387-29233-5. PMID 16626028. doi:10.1007/0-387-32957-9_5.
- ↑ Drews K, Bashir T, Dörries K (January 2000). "Quantification of human polyomavirus JC in brain tissue and cerebrospinal fluid of patients with progressive multifocal leukoencephalopathy by competitive PCR". Journal of Virological Methods 84 (1): 23–36. PMID 10644084. doi:10.1016/S0166-0934(99)00128-7.
- ↑ Nickeleit V, Hirsch HH, Binet IF, Gudat F, Prince O, Dalquen P, Thiel G, Mihatsch MJ (May 1999). "Polyomavirus infection of renal allograft recipients: from latent infection to manifest disease". Journal of the American Society of Nephrology 10 (5): 1080–9. PMID 10232695.
- ↑ Randhawa PS, Vats A, Zygmunt D, Swalsky P, Scantlebury V, Shapiro R, Finkelstein S (August 2002). "Quantitation of viral DNA in renal allograft tissue from patients with BK virus nephropathy". Transplantation 74 (4): 485–8. PMID 12352906. doi:10.1097/00007890-200208270-00009.
- ↑ Busam KJ, Jungbluth AA, Rekthman N, Coit D, Pulitzer M, Bini J, Arora R, Hanson NC, Tassello JA, Frosina D, Moore P, Chang Y (September 2009). "Merkel cell polyomavirus expression in merkel cell carcinomas and its absence in combined tumors and pulmonary neuroendocrine carcinomas". The American Journal of Surgical Pathology 33 (9): 1378–85. PMC 2932664. PMID 19609205. doi:10.1097/PAS.0b013e3181aa30a5.
- ↑ Tolstov YL, Pastrana DV, Feng H, Becker JC, Jenkins FJ, Moschos S, Chang Y, Buck CB, Moore PS (September 2009). "Human Merkel cell polyomavirus infection II. MCV is a common human infection that can be detected by conformational capsid epitope immunoassays". International Journal of Cancer 125 (6): 1250–6. PMC 2747737. PMID 19499548. doi:10.1002/ijc.24509.
- ↑ Pastrana DV, Tolstov YL, Becker JC, Moore PS, Chang Y, Buck CB (September 2009). "Quantitation of human seroresponsiveness to Merkel cell polyomavirus". PLOS Pathogens 5 (9): e1000578. PMC 2734180. PMID 19750217. doi:10.1371/journal.ppat.1000578.
- ↑ Carter JJ, Paulson KG, Wipf GC, Miranda D, Madeleine MM, Johnson LG, Lemos BD, Lee S, Warcola AH, Iyer JG, Nghiem P, Galloway DA (November 2009). "Association of Merkel cell polyomavirus-specific antibodies with Merkel cell carcinoma". Journal of the National Cancer Institute 101 (21): 1510–22. PMC 2773184. PMID 19776382. doi:10.1093/jnci/djp332.
- ↑ Elizabeth Matisoo-Smith; K. Ann Horsburgh (2012). DNA for Archaeologists. Routledge. ISBN 978-1598746815.
- ↑ Gross L (June 1953). "A filterable agent, recovered from Ak leukemic extracts, causing salivary gland carcinomas in C3H mice". Proceedings of the Society for Experimental Biology and Medicine 83 (2): 414–21. PMID 13064287. doi:10.3181/00379727-83-20376.
- ↑ Stewart SE, Eddy BE, Borgese N (June 1958). "Neoplasms in mice inoculated with a tumor agent carried in tissue culture". Journal of the National Cancer Institute 20 (6): 1223–43. PMID 13549981. doi:10.1093/jnci/20.6.1223.
- ↑ Eddy BE, Stewart SE (November 1959). "Characteristics of the SE polyoma virus". American Journal of Public Health and the Nation's Health 49 (11): 1486–92. PMC 1373056. PMID 13819251. doi:10.2105/AJPH.49.11.1486.
- ↑ Schowalter RM, Pastrana DV, Buck CB (July 2011). "Glycosaminoglycans and sialylated glycans sequentially facilitate Merkel cell polyomavirus infectious entry". PLOS Pathogens 7 (7): e1002161. PMC 3145800. PMID 21829355. doi:10.1371/journal.ppat.1002161.
- ↑ Gottlieb KA, Villarreal LP (June 2001). "Natural biology of polyomavirus middle T antigen". Microbiology and Molecular Biology Reviews 65 (2): 288–318; segunda e terceira páxinas, táboa de contidos. PMC 99028. PMID 11381103. doi:10.1128/mmbr.65.2.288-318.2001.
- ↑ Peretti A, FitzGerald PC, Bliskovsky V, Pastrana DV, Buck CB (January 2015). "Genome Sequence of a Fish-Associated Polyomavirus, Black Sea Bass (Centropristis striata) Polyomavirus 1". Genome Announcements 3 (1): e01476–14. PMC 4319505. PMID 25635011. doi:10.1128/genomeA.01476-14.
- ↑ López-Bueno A, Mavian C, Labella AM, Castro D, Borrego JJ, Alcami A, Alejo A (October 2016). "Concurrence of Iridovirus, Polyomavirus, and a Unique Member of a New Group of Fish Papillomaviruses in Lymphocystis Disease-Affected Gilthead Sea Bream". Journal of Virology 90 (19): 8768–79. PMC 5021401. PMID 27440877. doi:10.1128/JVI.01369-16.
